Спирива респимат (Spiriva respimat)
1-Z А Б В Г Д Е - Ж - З И - Й К Л М Н О П Р С Т У Ф Х Ц Ч - Щ Э Ю - Я
Бронхолитический препарат - блокатор м-холинорецепторов
Фармако-терапевтическая группа
М-холиноблокатор
Состав
Раствор для ингаляций прозрачный бесцветный или почти бесцветный. В 1 дозе содержится 3,1235 мкг тиотропия бромида моногидрата, что соответствует содержанию тиотропия 2,5 мкг. Вспомогательные вещества: бензалкония хлорид - 1.105 мкг, динатрия эдетат - 1.105 мкг, хлористоводородная кислота 1М - до pH 2.8-3.0, вода - до 11.05 мг.
Объем картриджа 4,5 мл (60 доз). В комплекте идет с ингалятором Респимат®. Упакованы в картонную пачку.
Показания к применению
Проведение поддерживающего лечения у больных ХОБЛ, в том числе показано при эмфиземе, сохраняющейся одышке, хроническом бронхите, и с целью предотвращения обострений; проведение дополнительного лечения пациентов, страдающих бронхиальной астмой, для снижения частоты обострений и симптоматики, а также улучшения качества жизни.
Противопоказания к применению
Возраст до 18 лет; первый триместр беременности; повышенная чувствительность к одному или сумме ингредиентов препарата.
С осторожностью: закрытоугольная глаукома; обструкция шейки мочевого пузыря; гиперплазия предстательной железы.
Возможные побочные эффекты
ВНИМАНИЕ! Если вы подозреваете, что при приеме препарата ваше самочувствие ухудшилось, появились какие-то побочные эффекты, нужно сразу же обратиться очно к врачу, назначившему препарат!
Многие из перечисленных ниже нежелательных реакций могут быть обусловлены м-холиноблокирующим свойствами препарата.
Побочные реакции были выявлены на основании данных, полученных при проведении клинических исследований и отдельных сообщений в течение пострегистрационного использования препарата.
Со стороны обмена веществ: дегидратация*.
Со стороны нервной системы: нечасто (?0.1% и <1%) - головокружение; бессонница*.
Со стороны органа зрения: редко (?0.01% и <0.1%) - повышение внутриглазного давления, глаукома, нечеткое зрение.
Со стороны сердечно-сосудистой системы: нечасто (>0.1% и <1%) - мерцательная аритмия, тахикардия (включая суправентрикулярную тахикардию), ощущение сердцебиения.
Со стороны органов дыхания: нечасто (?0.1% и <1%) - кашель, носовое кровотечение, фарингит, дисфония; редко (?0.01% и <0.1%) - парадоксальный бронхоспазм, ларингит; синусит*.
Со стороны пищеварительной системы: часто (?1% и <10%) - незначительная преходящая сухость слизистой оболочки глотки; нечасто (>0.1% и <1%) - запор, кандидоз полости рта, дисфагия; редко (?0.01% и <0.1%) - гастроэзофагеальный рефлюкс, гингивит, глоссит, стоматит; кишечная непроходимость, включая паралитическую кишечную непроходимость*.
Со стороны кожных покровов: редко (?0.01% и <0.1%) - кожные инфекции и язвы на коже, сухость кожи.
Аллергические реакции: нечасто (>0.1% и <1%) - сыпь, зуд; редко (?0.01% и <0.1%) - ангионевротический отек, крапивница; гиперчувствительность, включая реакции немедленного типа*.
Со стороны костно-мышечной системы и соединительной ткани: припухлость суставов*.
Со стороны мочевыделительной системы: нечасто (>0.1% и <1%) - дизурия, задержка мочи (чаще у мужчин с наличием предрасполагающих факторов); редко (?0.01% и <0.1%) - инфекция мочевыводящих путей.
* в объединенной базе клинических исследований данные побочные реакции не были выявлены; отмечены лишь единичные сообщения о данных побочных реакциях при широком применении препарата, однако связь с м-холиноблокирующим действием препарата не доказана; частоту этих редких явлений трудно оценить.
Применение при беременности и кормлении грудью
Данные о влиянии препарата Спирива® Респимат® на беременность ограничены. При изучении репродуктивной токсичности на животных не получено указаний на прямые или опосредованные неблагоприятные влияния препарата. В качестве меры предосторожности предпочтительнее воздержаться от применения препарата Спирива® Респимат® при беременности.
Клинических данных о влиянии тиотропия бромида в период грудного вскармливания нет.
Препарат не следует применять у беременных или кормящих грудью женщин, если только ожидаемая польза для матери превышает потенциальный риск для плода и ребенка. На период применения препарата необходимо прекратить кормление грудью ребенка.
Применение при нарушениях функции печени
У пациентов с нарушениями функции печени можно использовать препарат Спирива® Респимат® в рекомендуемой дозе.
Применение при нарушениях функции почек
У пациентов с незначительными нарушениями функции почек (КК 50-80 мл/мин) можно использовать препарат Спирива® Респимат® в рекомендуемой дозе.
Однако, использование препарата у пациентов с умеренными или значительными нарушениями функции почек (КК <50 мл/мин) должно тщательно мониторироваться.
Применение препарата у детей
Противопоказано назначение детям и подросткам в возрасте до 18 лет (ввиду отсутствия данных по эффективности и безопасности).
Применение у пожилых пациентов
У пациентов пожилого возраста можно использовать препарат Спирива® Респимат® в рекомендуемой дозе.
Дозировка, как принимать Спирива респимат
Рекомендуемая терапевтическая доза составляет 2 ингаляционные дозы спрея из ингалятора Респимат® (5 мкг/доза) 1 раз/сут, в одно и то же время дня.
При лечении бронхиальной астмы полный терапевтический эффект наступает через несколько дней.
У пациентов пожилого возраста, пациентов с нарушениями функции печени и пациентов с незначительными нарушениями функции почек (КК 50-80 мл/мин) можно использовать препарат Спирива® Респимат® в рекомендуемой дозе.
Однако использование препарата у пациентов с умеренными или значительными нарушениями функции почек (КК <50 мл/мин) должно тщательно мониторироваться.
ХОБЛ обычно не встречается у детей. Безопасность и эффективность применения препарата Спирива® Респимат® у детей не изучены.
Правила применения ингалятора Спирива® Респимат®
Вставка картриджа и подготовка к использованию
Перед первым использованием ингалятора необходимо осуществить действия, приведенные ниже под номерами 1-6.
1. При закрытом зеленом колпачке следует нажать стопорную кнопку и одновременно снять прозрачную гильзу, потянув ее вниз.
2. Вынуть картридж из упаковки. Вставить его узким концом в ингалятор до фиксации. Чтобы убедиться в том, что картридж полностью вставлен, следует сильно надавить картриджем на твердую поверхность. При этом дно картриджа не должно быть на одном уровне с нижним краем ингалятора, нижняя часть картриджа серебряного цвета должна быть видна. После того как картридж вставлен в ингалятор, не следует его вынимать.
3. Одеть снова прозрачную гильзу. После этого гильза не должна больше сниматься.
Подготовка к первому использованию ингалятора Спирива® Респимат®
4. Следует держать ингалятор Спирива® Респимат® вертикально с одетым зеленым колпачком. Нужно повернуть прозрачную гильзу в направлении красных стрелок, указанных на этикетке, до щелчка (пол-оборота).
5. Снять зеленый колпачок.
6. Направить ингалятор Спирива® Респимат® вниз. Нажать кнопку подачи дозы. Закрыть зеленый колпачок.
Следует повторить этапы 4, 5 и 6 до появления аэрозольного облачка.
Затем повторить этапы 4, 5 и 6 еще 3 раза, чтобы обеспечить подготовку ингалятора для применения.
Теперь ингалятор Спирива® Респимат® готов к применению.
Осуществление этих этапов не уменьшает число доз препарата. После подготовки ингалятор Спирива® Респимат® позволяет высвободить 30 доз (60 ингаляций).
Использование ингалятора Спирива® Респимат®
Следует использовать этот ингалятор только 1 раз/сут. Каждый раз необходимо делать 2 ингаляции.
I. Держать ингалятор Спирива® Респимат® вертикально с одетым зеленым колпачком, чтобы предотвратить случайное высвобождение лекарства. Повернуть прозрачную гильзу по направлению красных стрелок, указанных на этикетке, до щелчка (пол-оборота).
II. Снять зеленый колпачок. Выдохнуть медленно и глубоко. Охватить плотно губами конец мундштука. Воздушное отверстие ингалятора должно быть при этом свободно. Направить ингалятор к задней части глотки.
Во время медленного и глубокого вдоха через рот следует нажать кнопку подачи дозы и продолжать вдох как можно дольше. Задержать дыхание на 10 секунд или так долго, как удобно.
III. Повторить этапы I-II, чтобы получить полную дозу. Следует использовать этот ингалятор только 1 раз/сут. Каждый раз необходимо делать 2 ингаляции.
Закрыть зеленый колпачок ингалятора до его следующего применения.
Если ингалятор Спирива® Респимат® не использовался более 7 дней, следует направить его перед применением вниз и нажать 1 раз на кнопку подачи дозы. Если ингалятор не использовался более чем 21 день, повторить этапы 4-6 до получения аэрозольного облачка. Затем повторить этапы 4-6 еще три раза.
Определение момента, когда нужно начать пользоваться новым ингалятором
Ингалятор Спирива® Респимат® содержит 30 доз (60 ингаляций). Указатель доз показывает, сколько примерно препарата еще осталось. Когда указатель ингалятора покажет на красную область шкалы, это означает, что лекарства осталось примерно на 7 дней (14 ингаляций). В этот промежуток времени необходимо получить рецепт на новый ингалятор Спирива® Респимат®.
Когда указатель ингалятора достигнет конца красной области шкалы (т.е. когда использовано 30 доз), это означает, что ингалятор Спирива® Респимат® пуст. Произойдет автоматическое блокирование ингалятора. С этого момента времени поворот прозрачной гильзы будет невозможен.
После первого использования ингалятор Спирива® Респимат® следует утилизировать не позднее, чем через 3 месяца, даже если не все количество лекарства было применено.
Уход за ингалятором
Мундштук и металлическую часть распылителя необходимо чистить влажной мягкой тканевой салфеткой, как минимум, 1 раз в неделю.
Небольшое обесцвечивание мундштука не влияет на функционирование ингалятора. При необходимости вытирать ингалятор также и снаружи влажной тканевой салфеткой.
Дополнительные указания при приеме Спирива респимат
Препарат Спирива® Респимат®, как бронходилататор, применяемый 1 раз/сут для поддерживающего лечения, не следует применять в качестве начальной терапии при острых приступах бронхоспазма или для устранения остро возникающих симптомов. В случае развития острого приступа используются быстродействующие ?2-агонисты.
Препарат Спирива® Респимат® не следует применять для лечения бронхиальной астмы в качестве терапии первой линии. Пациентам следует рекомендовать на фоне приема препарата Спирива® Респимат® продолжать противовоспалительную терапию (например, ингаляционными ГКС), даже если симптомы уменьшатся.
После применения препарата могут развиваться немедленные реакции повышенной чувствительности.
Ингаляция препарата может вызывать бронхоспазм.
При умеренной или выраженной почечной недостаточности (КК ?50 мл/мин) прием препарата следует вести под тщательным наблюдением, как и при приеме всех лекарственных препаратов, экскретируемых преимущественно почками.
Перед началом применения пациенты должны быть ознакомлены с инструкцией по применению.
Не следует допускать попадания раствора или аэрозоля в глаза. Боль или дискомфорт в глазах, нечеткое зрение, зрительные ореолы в сочетании с покраснением глаз, отек конъюнктивы и роговицы могут быть симптомами острой закрытоугольной глаукомы. При развитии любой комбинации этих симптомов следует немедленно обратиться к специалисту. Глазные капли, обладающие миотическим действием, не считаются эффективным лечением.
Спирива® Респимат® не следует использовать чаще, чем 1 раз/сут.
Картриджи Спирива® следует использовать только с ингалятором Респимат®.
Влияние на способность к вождению автотранспорта и управлению механизмами
Исследования по изучению влияния на способность управлять транспортными средствами и механизмами не проводились. Следует соблюдать осторожность при выполнении данных видов деятельности, т.к. возможно развитие головокружения или нечеткости зрения.
У больных с конвульсивной анамнезией Ципрофлоксоацин следует применять после подходящей антиконвульсивной терапии . У некоторых водителей или работающих на машинах возможно ослабление реакций во время лечения, причем алкоголь может повысить влияние неблагоприятных эффектов. Таблетки необходимо применять с определенным количеством воды. При примении препарата на голодный желудок ускоряется процесс всасывания. Учитывая чувствительность препарата к свету, его надо хранить внутри внешней упаковки в темном месте.
Взаимодействие с другими лекарственными препаратами. Антациды, содержащие магний и алюминий, замедляют процесс высасывания препарата. Ципрофлоксацин надо принимать за два часа до приема или через два часа после приема антицитов. При одновременном применении ципрофлоксацина и теофилина возможно повышение концентрации крови, вызванного теофилином. В таких случаях необходимо регулировать дозу теофилина. Во избежание повышенной алкализации мочи и с учетом риска кристаллурии следует обратить внимание на прием жидкостей в достаточном количестве.
Передозировка
При применении препарата в высоких дозах возможны проявления м-холиноблокирующего действия. После 14-дневного ингаляционного применения тиотропия бромида в дозах, достигавших 40 мкг, у здоровых лиц не наблюдалось значимых неблагоприятных явлений, кроме чувства сухости слизистых оболочек носа и ротоглотки, частота которых зависела от величины дозы (10-40 мкг/сут). Исключение составляло отчетливое снижение саливации, начиная с 7 дня применения препарата. В шести долгосрочных исследованиях у пациентов с ХОБЛ при ингаляционном применении раствора тиотропия бромида в суточной дозе 10 мкг в течение 4-48 недель не наблюдалось существенных нежелательных явлений.
Вследствие низкой пероральной биодоступности возникновение острой интоксикации в случае непреднамеренного проглатывания раствора тиотропия бромида для ингаляций из картриджа маловероятно.
Как хранить препарат
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°С. Препарат необходимо использовать в течение 3 месяцев после первой ингаляции. Срок годности - 3 года.
Условия отпуска
Препарат отпускается по рецепту.
Информация для врачей о препарате Спирива респимат
Фармакодинамика
Бронхолитический препарат.
Тиотропия бромид - м-холиноблокатор длительного действия. Препарат обладает одинаковым сродством к M1-М5 подтипам мускариновых рецепторов. Результатом ингибирования М3-рецепторов в дыхательных путях является расслабление гладкой мускулатуры. Бронходилатирующий эффект зависит от дозы и сохраняется не менее 24 ч. Значительная продолжительность действия связана, вероятно, с очень медленной диссоциацией препарата от М3-рецепторов; период полудиссоциации существенно более длительный, чем у ипратропия бромида.
При ингаляционном способе введения тиотропия бромид, как N-четвертичное производное аммония, оказывает местный избирательный эффект (на бронхи), при этом в терапевтических дозах не вызывает системных м-холиноблокирующих побочных эффектов. Диссоциация от М2-рецепторов происходит быстрее, чем от М3-рецепторов, что свидетельствует о преобладании селективности в отношении М3 подтипа рецепторов над М2-рецепторами. Высокое сродство к рецепторам и медленная диссоциация препарата из связи с рецепторами обусловливают выраженный и продолжительный бронходилатирующий эффект у пациентов с ХОБЛ.
Бронходилатация, развивающаяся после ингаляции тиотропия бромида, обусловлена, в первую очередь, местным (на дыхательные пути), а не системным действием.
В клинических исследованиях было показано, что применение препарата Спирива®Респимат® 1 раз/сут приводит к значительному улучшению (по сравнению с плацебо) функции легких (объем форсированного выдоха за 1 секунду ОФВ1 и форсированная жизненная емкость легких ФЖЕЛ) в течение 30 мин после использования первой дозы. Улучшение функции легких сохраняется в течение 24 ч при равновесной концентрации.
Фармакодинамическое равновесие достигалось в течение одной недели. Спирива®Респимат® значительно улучшал утреннюю и вечернюю пиковую объемную скорость выдоха (ПОСВ), измеренную больными. Применение препарата Спирива®Респимат® приводило к уменьшению (по сравнению с плацебо) использования бронходилататора в качестве средства скорой помощи. Бронходилатирующий эффект препарата сохраняется на протяжении 48 недель применения препарата; признаков привыкания не отмечается.
Анализ комбинированных данных двух рандомизированных, плацебо-контролируемых, перекрестных клинических исследований показал, что бронходилатирующий эффект препарата Спирива® Респимат® (5 мкг) после 4-недельного периода лечения был в количественном отношении выше, чем эффект препарата Спирива® (18 мкг).
В долгосрочных (12-месячных) исследованиях было установлено, что Спирива®Респимат® значительно уменьшает одышку; улучшает качество жизни; снижает психосоциальное воздействие ХОБЛ и увеличивает активность.
Препарат Спирива® Респимат® достоверно улучшал общее состояние здоровья (общий балл) по сравнению с плацебо к концу двух 12-месячных исследований, это различие сохранялось на протяжении всего периода лечения; препарат Спирива®Респимат® значительно уменьшал число обострений ХОБЛ, и увеличивал период до момента первого обострения по сравнению с плацебо.
Доказано, что Спирива® Респимат® уменьшает риск обострения ХОБЛ и значительно снижает количество случаев госпитализации.
При ретроспективном анализе отдельных клинических исследований было замечено статистически недостоверное увеличение, по сравнению с плацебо, количества случаев смерти у пациентов с нарушениями ритма сердца. Однако эти данные статистически не подтверждены и могут быть связаны с заболеванием сердца.
В клинических исследованиях у пациентов, страдающих бронхиальной астмой и продолжающих испытывать симптомы заболевания, несмотря на поддерживающую терапию ингаляционным ГКС, в т.ч. в комбинации с длительно действующим
агонистом бета2-адренорецепторов, было установлено, что добавление препарата Спирива® Респимат® к поддерживающей терапии приводило к достоверному улучшению функции легких по сравнению с плацебо, значительно уменьшало число серьезных обострений и периодов ухудшения симптомов бронхиальной астмы, увеличивало период до первого их наступления, приводило к достоверному улучшению качества жизни и увеличению числа пациентов с положительным ответом на поддерживающую терапию.
Бронходилатирующий эффект препарата сохранялся на протяжении 1 года применения, признаков привыкания не отмечалось.
Фармакокинетика
Тиотропия бромид - четвертичное производное аммония, умеренно растворимое в воде. Тиотропия бромид выпускается в виде раствора для ингаляций, который применяется с помощью ингалятора Респимат®. Приблизительно 40% от величины ингаляционной дозы осаждается в легких, остальное количество поступает в ЖКТ. Некоторые фармакокинетические данные, описанные ниже, были получены при использовании доз, превышающих рекомендуемые для лечения.
Всасывание
После ингаляции раствора молодыми здоровыми добровольцами установлено, что в системную циркуляцию поступает около 33% от величины ингаляционной дозы. Прием пищи не влияет на всасывание тиотропия бромида, в связи с тем, что он плохо всасывается из ЖКТ. Абсолютная биодоступность при приеме внутрь составляет 2-3%. Cmax в плазме наблюдается через 5 мин после ингаляции.
Распределение
Связывание препарата с белками плазмы составляет 72%; Vd - 32 л/кг. На стадии динамического равновесия пиковая концентрация тиотропия бромида в плазме у пациентов с ХОБЛ составляет 10.5-11.7 пг/мл через 10 мин после применения препарата в дозе 5 мкг с помощью ингалятора Респимат®. На стадии динамического равновесия Cmax тиотропия бромида в плазме у пациентов с бронхиальной астмой составляет 5.15 пг/мл через 5 мин после приема в той же дозе с помощью ингалятора Респимат®. На стадии динамического равновесия наименьшая концентрация в плазме составила 1.49-1.68 пг/мл. Исследования показали, что тиотропия бромид не проникает через ГЭБ.
Метаболизм
Степень биотрансформации незначительна. Это подтверждается тем, что после в/в введения препарата молодым здоровым добровольцам в моче обнаруживается 74% субстанции тиотропия бромида в неизмененном виде. Тиотропия бромид является эфиром, который расщепляется на этанол-N-метилскопин, и дитиенилгликолиевую кислоту; эти соединения не связываются с мускариновыми рецепторами.
В исследованиях in vitro показано, что некоторая часть препарата (< 20% от дозы после в/в введения) метаболизируется путем окисления цитохромом Р450 с последующей конъюгацией с глютатионом и образованием различных метаболитов. Данный механизм может тормозиться ингибиторами изоферментов CYP 2D6 и 3А4 (хинидин, кетоконазол и гестоден). Таким образом, CYP2D6 и 3А4 участвуют в метаболизме препарата. Тиотропия бромид даже в сверхтерапевтических концентрациях не ингибирует цитохромом Р450 1А1, 1А2, 2В6, 2С9, 2С19, 2D6, 2Е1 или 3А в микросомах печени человека.
Выведение
Терминальный T1/2 тиотропия бромида после ингаляции составляет 5-6 дней у здоровых добровольцев и пациентов с ХОБЛ. У пациентов с бронхиальной астмой эффективный Т1/2 после ингаляции составляет 34 ч.
Общий клиренс после в/в введения препарата молодым здоровым добровольцам составлял 880 мл/мин, при индивидуальной вариабельности 22%. Тиотропия бромид после в/в введения в основном выводится почками в неизмененном виде (74%). После ингаляции раствора у здоровых добровольцев почечная экскреция составляет 20.1-29.4%, оставшаяся неабсорбировавшаяся часть выводится через кишечник. В стадии фармакокинетического равновесия у пациентов с астмой 11.9% (0.595 мкг) дозы выводится в неизменном виде с мочой через 24 ч после приема препарата. Почечный клиренс тиотропия бромида превышает КК, что свидетельствует о его канальцевой секреции. После длительного ингаляционного приема препарата 1 раз/сут пациентами с ХОБЛ фармакокинетические равновесие достигается на 7 день; при этом в дальнейшем не наблюдаемся кумуляции.
Тиотропия бромид имеет линейную фармакокинетику в терапевтических пределах после в/в применения, ингаляции сухого порошка и ингаляции раствора.
Фармакокинетика в особых клинических случаях
В пожилом возрасте отмечается снижение почечного клиренса тиотропия бромида (326 мл/мин у пациентов с ХОБЛ в возрасте до 58 лет и 163 мл/мин у пациентов с ХОБЛ старше 70 лет), что, возможно, объясняется снижением функции почек. Экскреция тиотропия бромида с мочой после ингаляционного применения снижается с 14% у молодых здоровых добровольцев примерно до 7% у пациентов с ХОБЛ, однако концентрация в плазме у пациентов пожилого возраста с ХОБЛ существенно не изменялась, если учитывать меж- и внутрииндивидуальную вариабельность (после ингаляции сухого порошка AUC увеличивалась на 43%). Установлено, что у пациентов с бронхиальной астмой воздействие тиотропия бромида не зависит от возраста пациентов.
Небольшие нарушения функции почек (КК 50-80 мл/мин), которые могут наблюдаться у пациентов пожилого возраста, сопровождаются незначительным увеличением концентрации тиотропия бромида в плазме (после в/в инфузии AUC увеличивалась на 39%). У пациентов с ХОБЛ и умеренными или значительными нарушениями функции почек (КК<50 мл/мин) в/в применение тиотропия бромида приводило к двукратному увеличению концентрации в плазме (AUC увеличивалась на 82%), аналогичное повышение концентрации в плазме отмечалось и после ингаляции сухого порошка.
У пациентов с бронхиальной астмой и небольшими нарушениями функции почек (КК 50-80 мл/мин) ингаляционное применение тиотропия бромида не приводило к значительному увеличению воздействия в сравнении с пациентами с нормальной функцией почек.
Предполагается, что печеночная недостаточность не оказывает значительного влияния на фармакокинетику тиотропия бромида, т.к. тиотропия бромид преимущественно выводится почками.
Взаимодействие с другими веществами
Хотя специальных исследований лекарственного взаимодействия не проводилось, тиотропия бромид применялся совместно с другими препаратами, применяющимися для лечении ХОБЛ, включая симпатомиметические бронходилататоры, метилксантины, ГКС для приема внутрь и ингаляционного применения, антигистаминные препараты, муколитики, модификаторы лейкотриенов, кромоны, анти-IgE препараты; при этом клинических признаков лекарственного взаимодействия не отмечалось.
Длительное совместное применение тиотропия бромида с другими м-холиноблокирующими препаратами не изучалось. Поэтому долгосрочное совместное применение препарата Спирива® Респимат® с другими м-холиноблокирующими препаратами не рекомендуется.

Секреты долголетия: уроки из синих зон Земли

Влияние микропластика на здоровье: что говорят эксперты

Новый подход к менопаузе: заморозка ткани яичника может изменить все

Омега-3 vs. витамин D: что выбрать для здоровья иммунной системы?

Сможем ли мы добавить больше активной жизни к нашим годам?

Новое исследование: как фантазии помогают укрепить память
 Беременность и варикоз
Беременность и варикоз Бандаж и ортез голеностопный
Бандаж и ортез голеностопный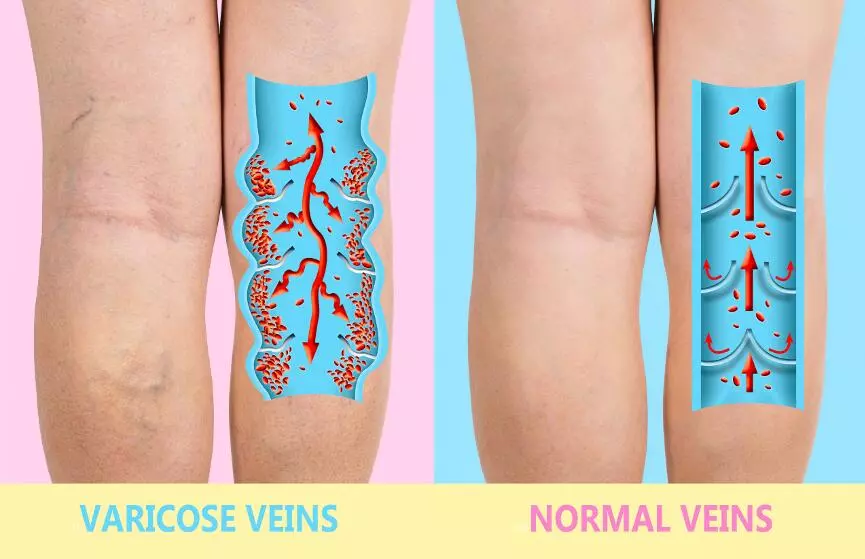 Варикозное расширение вен
Варикозное расширение вен Воспаление копчикового хода
Воспаление копчикового хода

