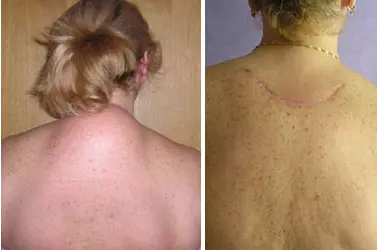
Иларис® (Ilaris®)
1-Z А Б В Г Д Е - Ж - З И - Й К Л М Н О П Р С Т У Ф Х Ц Ч - Щ Э Ю - Я
Клинико-фармакологическая форма - канакинумаб
Форма выпуска
Лиофилизат для приготовления раствора для подкожного введения, 150 мг.
Описание препарата Иларис® (Ilaris®)
Лиофилизат: лиофилизированный порошок белого цвета.
Растворитель: прозрачная бесцветная жидкость.
Состав
1 флакон лиофилизата для приготовления раствора для подкожного введения содержит:
действующее вещество: канакинумаб 150 мг;
вспомогательные вещества: L-гистидин 2,801 мг, L-гистидина гидрохлорид моногидрат 1,673 мг, полисорбат-80 0,60 мг, сахароза 92,35 мг, кислота хлористоводородная 1 М до pH 6,5.
Если комплектность предполагает включение растворителя: 1 флакон растворителя содержит: вода для инъекций - 5 мл.
Показания к применению
Острый подагрический артрит
Лечение частых острых приступов подагрического артрита и предупреждение развития новых приступов при неэффективности, непереносимости или при наличии противопоказаний к применению нестероидных противовоспалительных препаратов и/или колхицина и при невозможности проведения терапии повторными курсами глюкокортикостероидов.
Криопирин-ассоциированный периодический синдром (CAPS) у взрослых и детей в возрасте >2 лег и старше, включая:
- семейный холодовой аутовоспалительный синдром (FCAS)/ Семейная холодовая крапивница (FCU);
- синдром Макл-Уэльса (MWS);
- младенческое мультисистемное воспалительное заболевание (NOMID) / хронический младенческий неврологический кожно-артикулярный синдром (CINCA).
Активная фаза системного ювенильного идиопатического артрита (сЮИА) у детей в возрасте >2 лет и старше.
Противопоказания к применению
- Повышенная чувствительность к активному веществу или другим компонентам препарата в анамнезе;
- острые инфекционные заболевания;
- беременность и период грудного вскармливания;
- дети младше 2 лет (безопасность и эффективность для указанной категории пациентов изучены не достаточно).
Возможные побочные эффекты
ВНИМАНИЕ! Если вы подозреваете, что при приеме препарата ваше самочувствие ухудшилось, появились какие-то побочные эффекты, нужно сразу же обратиться очно к врачу, назначившему препарат!
При применении препарата Иларис® в ходе клинических исследований отмечалось повышение частоты инфекционных заболеваний, преимущественно инфекций верхних дыхательных путей. Течение инфекционных заболеваний чаще всего было легким или средней степени тяжести, однако отмечались и случаи тяжелого течения инфекционных заболеваний. Наблюдались изолированные случаи развития редких или оппортунистических инфекций на фоне приема препарата Иларис®, однако, связь данных заболеваний с приемом препарата не известна.
Для оценки частоты нежелательных явлений (НЯ), выявленных в плацебо-контролируемых клинических исследованиях (при применении препарата для лечения криопирин-ассоциированного периодического синдрома в дозе 150 мг при массе тела >40 кг и 2 мг/кг при массе тела >15 кг и <40 кг и при лечении сЮИА у пациентов в возрасте от 2 до 20 лет) и для лечения острых приступов подагрического артрита в дозах от 10 мг до 300 мг в активно контролируемых иссследованиях, использованы следующие критерии (согласно классификации ВОЗ): очень частые (>1/10 назначений); частые (>1/100, <1/10); нечастые (>1/1000, <1/100); редкие (>1/10000, <1/1000); очень редкие (< 1/10000), частота неизвестна (недостаточно данных для оценки частоты развития). **
Подагрический артрит
Инфекционные и паразитарные заболевания: очень часто - инфекции (в частности, назофарингит, синусит, вирусные инфекции верхних дыхательных путей, бронхит, пневмония, фарингит, грипп, инфекции мочевыводящих путей, инфекции уха, гастроэнтерит, панникулит).
Нарушения со стороны нервной системы: часто - головокружение/вертиго.Нарушения со стороны костно-мышечной системы: часто - боль в спине.
Нарушения со стороны пищеварительной системы: нечасто - гастроэзофагеальная рефлюксная болезнь.
Общие нарушения и реакции в месте введения: часто - общая слабость/повышенная утомляемость.
Реакции в месте введения препарата наблюдались у 1,2% пациентов, получавших лечение препаратом Иларис® в клинических исследованиях.
Изменения лабораторных показателей
Общий анализ крови
Снижение количества лейкоцитов <0,8х109/л нижней границы нормы отмечалось у 6,7% пациентов получавших лечение препаратом Иларис® по сравнению с 1,4% пациентов, получавших триамцинолон. Снижение абсолютного количества нейтрофилов ниже 1 х 109 /л отмечалось у 2% пациентов в сравнительных исследованиях по подагрическому артриту. Наблюдались также изолированные случаи снижения количества нейтрофилов ниже 0,5 х 109 /л.
В 12,7% случаев на фоне терапии канакинумабом наблюдалось легкое и преходящее снижение количества тромбоцитов (в пределах от 75 х109/л) до нижней границы нормы (у препарата сравнения данное снижение наблюдалось в 7,7% случаев).
Мочевая кислота
На фоне терапии канакинумабом наблюдается преходящее повышение концентрации мочевой кислоты (примерно на 0,6 мг/дл). Препарат Иларис® не уменьшает способность противоподагрических средств снижать концентрацию мочевой кислоты при совместном применении.
Аспартатаминотрасфераза/аланинаминотрансфераза (АСТ/АЛТ)
На фоне терапии канакинумабом возможно развитие слабо и умеренно выраженного повышения активности АСТ/АЛТ.
Триглицериды
На фоне терапии канакинумабом, в среднем, наблюдается повышение концентрации триглицеридов в плазме крови на 33,5 мг/дл, а в группе применения триамцинолона - незначительное снижение на 3,1 мг/дл. Повышение концентрации триглицеридов более чем в 5 раз (по сравнению с верхней границей нормы) отмечалось в 2,4% случаев в группе применения канакинумаба и в 0,7% случаев в группе применения триамцинолона. Клиническая значимость данного наблюдения неизвестна.
Криопирин-ассоциированный периодический синдром
Инфекционные и паразитарные заболевания: очень часто - назофарингит; часто - инфекции мочевыводящих путей; инфекции верхних дыхательных путей, вирусная инфекция.
Нарушения со стороны нервной системы: очень часто - головокружение/вертиго*.
Нарушения со стороны кожи и подкожных тканей: очень часто - реакция в месте введения препарата**.
*Симптомы вертиго, в некоторых случаях, рассматривались как серьезные НЯ, все эпизоды вертиго разрешались, несмотря на продолжение терапии препаратом.
** Нежелательное явление (НЯ) было выявлено с помощью опросника для врача.
В ходе длительных, открытых исследований с эскалацией дозы отмечалось повышение частоты инфекционных заболеваний (гастроэнтерит, инфекции дыхательных путей и инфекции верхних дыхательных путей), тошноты и головокружения в группе пациентов, получающих дозы препарата 600 мг или 8 мг/кг, по сравнению с группами, получающими другие дозы препарата.
Изменения лабораторных показателей
Общий анализ крови
При применении препарата в клинических исследованиях у пациентов с CAPS отмечалось повышение гемоглобина и снижение числа лейкоцитов, нейтрофилов и тромбоцитов. Однако данные изменения были, вероятно, связаны со снижением выраженности воспалительного процесса на фоне терапии препаратом и не имели клинической значимости.
Ферменты печени
В редких случаях у больных с CAPS, получавших лечение препаратом, наблюдалось повышение активности "печеночных" трансаминаз.
Билирубин
В ряде случаев на фоне терапии препаратом у пациентов с CAPS отмечалось бессимптомное незначительное увеличение содержания билирубина в сыворотке крови, не сопровождающееся повышением активности "печеночных" трансаминаз.
сЮИА
Инфекционные и паразитарные заболевания: очень часто - инфекции (в частности, назофарингит, вирусные инфекции верхних дыхательных путей, пневмония, ринит, фарингит, тонзиллит, синусит, инфекции мочевыводящих путей, гастроэнтерит, вирусная инфекция).
Нарушения со стороны пищеварительной системы: очень часто - боль в верхней части живота.
Нарушения со стороны кожи и подкожных тканей: очень часто - реакция в месте введения препарата легкой степени тяжести*, часто - реакция в месте введения препарата средней степени тяжести*.
* - не приводило к прекращению исследования.
Изменения лабораторных показателей
Общий анализ крови
Снижение числа лейкоцитов <0,8х109/л нижней границы нормы отмечалось у 10,4% пациентов, получавших лечение препаратом Иларис®, по сравнеиию с 4,0% в группе плацебо.
Транзиторное снижение абсолютного количества нейтрофилов <1x109/л отмечалось у 6,0% пациентов, получавших лечение препаратом Иларис®, по сравнению с 2,0% в группе плацебо. Отмечался одни случай снижения абсолютного количества нейтрофилов <0,5х109/л при лечении препаратом Иларис®.
Умеренное и транзиторное снижение в пределах от 75 х109/л до нижней границы нормы тромбоцитов отмечалось у 6,3% пациентов, получавших препарат Иларис®, по сравнению с 2,0% в группе плацебо.
Ферменты печени
Трехкратное повышение АЛТ и /или ACT по сравнению с верхней границей нормы отмечалось у 4,1 % пациентов, получавших лечение препаратом Иларис®, по сравнению с 2,0% в группе плацебо. При последующем обследовании отмечалась нормализация показателей.
Реакции гиперчувствительности
При применении препарата Иларис® в клинических исследованиях сообщалось о нежелательных явлениях, расцененных врачами как реакции гиперчувствительности. В большинстве случаев данные реакции были выражены в легкой степени. При применении препарата не наблюдалось развития анафилактоидных или анафилактических реакций. Однако, при назначении препарата Иларис® нельзя исключить риск развития тяжелых реакций гиперчувствительности, которые могут отмечаться при инъекционном введении препаратов белкового происхождения. У пациентов, получавших лечение препаратам Иларис® по поводу подагрического артрита, CAPS и сЮИА выявлялись антитела к препарату в 1,5%, 3% и 2% случаев, соответственно. Взаимосвязи между образованием антител, клиническим ответом и развитием нежелательных явлений не выявлено.
Применение у больных в возрасте < 18 лет (пациенты с CAPS)
У детей в возрасте от 2 до 17 лет не наблюдалось клинически значимых отличий в безопасности и переносимости препарата Иларис®, включая общую частоту и тяжесть инфекций, в сравнении с общей популяцией больных. Наиболее часто у детей наблюдались инфекции верхних дыхательных путей.
Применение у больных > 65 лет
Не было выявлено различий в профиле безопасности препарата у данной группы больных.
Пациент должен быть информирован необходимости обращения к врачу в случае развития сильных побочных реакций, в том числе неуказанных в инструкции.
Дозировка, как принимать Иларис® (Ilaris®)
Препарат (лиофилизат) растворяют в 1 мл воды для инъекций (см. раздел "Указания по применению").
Инъекции проводят подкожно в те участки тела, где есть подкожно-жировая клетчатка: в живот, переднюю поверхность бедер, заднебоковую поверхность плеч.
Подагрический артрит
Рекомендованная доза препарата у взрослых 150 мг, препарат вводят во время приступа подагрического артрита, одномоментно подкожно. Для достижения максимальной эффективности препарат необходимо вводить как можно раньше после начала приступа подагрического артрита.
Пациентам, которые не ответили на первую инъекцию препарата Иларис®, повторно вводить препарат не следует. Пациентам, ответившим на лечение, повторное введение препарата Иларис® возможно, как минимум, через 12 недель после предыдущей инъекции.
Применять препарат Иларис® для терапии приступов подагрического артрита следует по мере необходимости. Оптимизирование контроля гиперурекимии следует проводить с помощью соответствующих противоподагрических препаратов.
Терапия препаратом может быть инициирована и проводится только врачом, имеющим опыт диагностики и лечения пациентов с подагрическим артритом.
Криопирин-ассоциированный периодический синдром
Рекомендованные стартовые дозы препарата Иларис® для пациентов с криопирин-ассоциированным периодическим синдромом:
Взрослым и детям > 4 лет в зависимости от массы тела назначают:
- пациентам с массой тела >40 кг - 150 мг;
- пациентам с массой тела >15 кг и <40кг - 2мг/кг;
-пациентам с массой тела >7,5 кг и <15кг - 4мг/кг.
Детям в возрасте от 2 лет и <4 лет с массой тела >7,5 кг препарат применяют из расчета 4 мг/кг.
Препарат вводят подкожно (п/к) 1 инъекция с интервалом 8 недель.
Если у пациентов при стартовой дозе 150 мг или 2 мг/кг не получен удовлетворительный клинический ответ, а именно процесс разрешения сыпи и других симптомов воспаления не наблюдается в течение 7-ми дней после первой инъекции препарата Иларис®, возможно проведение второй инъекции препарата в дозе 150 мг (при массе тела >40 кг) и 2 мг/кг (при массе тела >15 кг и <40 кг).
При достижении в последующем полного клинического ответа данным пациентам рекомендуется поддерживающая терапия препаратом Иларис® в дозе 300 мг 1 инъекция с интервалом 8 недель (при массе тела >40 кг) и 4 мг/кг 1 инъекция с интервалом 8 недель (при массе тела >15 кг и <40 кг).
Если удовлетворительный клинический эффект не наблюдается в течение 7 дней после повышения дозы, возможно проведение третьей инъекции препарата Иларис® в дозе 300 мг 1 инъекция с интервалом 8 недель (при массе тела > 40 кг) или 4 мг/кг (при массе тела >15 кг и <40 кг). При достижении в последующем полного клинического ответа данным пациентам рекомендуется поддерживающая терапия препаратом Иларис® в дозе 600 мг 1 инъекция с интервалом 8 недель (при массе тела > 40 кг) или 8 мг/кг (при массе тела >15 кг и <40 кг) 1 инъекция с интервалом 8 недель.
Если у пациентов при стартовой дозе 4 мг/кг удовлетворительный клинический эффект не наблюдается в течение 7 дней после первой инъекции, возможно проведение второй инъекции препарата Иларис® в дозе 4 мг/кг. При достижении в последующем полного клинического ответа данным больным рекомендуется поддерживающая терапия препаратом в дозе 8 мг/кг 1 инъекция с интервалом 8 недель.
Клинический опыт применения препарата с интервалом дозирования менее 4-х недель или в дозе более 600 мг или 8 мг/кг ограничен.
Повышение дозы препарата Иларис® требовалась наиболее часто для пациентов сNOMID/CINCA по сравнению с FCAS или MWS.
Терапия препаратом может быть инициирована и проводится только врачом, имеющим опыт диагностики и лечения пациентов с CAPS.
сЮИА
При сЮИА рекомендованная доза у пациентов с массой тела >7,5 кг составляет 4 мг/кг (с увеличением до 300 мг) каяцые 4 недели в виде подкожной инъекции.
После обучения технике подкожных инъекций, пациенты или лица, за ними ухаживающие, могут самостоятельно вводить препарат под надлежащим контролем (если врач сочтет это необходимым). Пациенты или лица, ухаживающие за ними, должны быть проинструктированы по технике приготовления раствора, шприцам и иглам, пригодным для проведения инъекции.
Применение у разных групп пациентов
Пациенты в возрасте > 65 лет
Не требуется коррекции дозы препарата у пациентов в возрасте > 65 лет.
Пациенты в возрасте < 18 лет
Подагрический артрит
Нет данных по применению препарата Иларис® для лечения подагрического артрита у детей и подростков < 18 лет.
Криопирин-ассоциированный периодический синдром с ЮИА
Опыт применения канакинумаба у детей младше 2 лет ограничен.
Пациенты с нарушением функции почек
Не требуется коррекции дозы препарата у пациентов с нарушениями функции почек (опыт клинического применения у таких пациентов ограничен).
Пациенты с нарушением функции печени
У пациентов с нарушениями функции печени эффективность и безопасность применения препарата не изучались. Так как препарат Иларис® - человеческий IgG, предполагается, что печеночная недостаточность не влияет на фармакокинетику данного препарата.
Влияние на беременность
Имеются ограниченные данные по применению препарата Иларис® у пациенток репродуктивного возраста и у беременных пациенток. В исследованиях на животных у препарата не было выявлено какой-либо репродуктивной токсичности. Женщинам следует применять надежные методы контрацепции во время терапии препаратом Иларис® и в течение 3 месяцев после применения последней дозы препарата.Неизвестно, проникает ли канакинумаб в грудное молоко. При необходимости применения препарата грудное вскармливание следует прекратить.
Управление транспортом
Пациентам, у которых на фоне применения препарата Иларис® возникает вертиго, следует воздержаться от управления транспортными средствами или механизмами до полного исчезновения данного нежелательного явления.
Дополнительные указания при приеме Иларис®
Опыт применения препарата Иларис® у пациентов с CAPS без установленной мутации в NLRP3 гене ограничен.
Нейтропения
На фоне терапии ингибиторами ИЛ-1, включая препарат Иларис®, нейтропения (абсолютное число нейтрофилов (АЧН) ниже 1.5х109) в основном отмечалась у пациентов с другими заболеваниями, а не у пациентов с различными фенотипами CAPS. До начала лечения препаратом, через 1-2 месяца после начала и периодически во время терапии препаратом необходимо проводить стандартные общеклинический анализ крови с целью выявления нейтропении. У пациентов с нейтропенией лечение препаратом Иларис® следует начинать только после нормализации числа нейтрофилов. При выявлении снижения АЧН на фоне терапии препаратом следует обеспечить надлежащий контроль состояния пациентов и при необходимости рассмотреть вопрос о прекращении лечения препаратом.
Злокачественные новообразования
Имеются сообщения о случаях развития злокачественных новообразований у пациентов, получающих терапию препаратом Иларис®, однако риск развития злокачественных новообразований на фоне терапии антителами, связывающими ИЛ-1 неизвестен.
Инфекционные заболевания
Применение препарата Иларис® может сопровождаться увеличением частоты серьезных инфекций, поэтому пациенты должны находиться под наблюдением врача, с целью выявления симптомов инфекции во время и после терапии препаратом.
Лечение препаратом Иларис® не следует начинать или продолжать у пациентов с активной инфекцией. При применении препарата Иларис® отмечались единичные случаи оппортунистических инфекций (в т.ч. аспергиллез, атипичные инфекционные заболевания микобактериальной этиологии, опоясывающий лишай). Невозможно исключить причинно-следственную связь между данными явлениями и применением препарата.
При применении препарата приблизительно у 12% пациентов с различными фенотипами CAPS наблюдались положительные результаты туберкулиновой пробы без каких- либо признаков туберкулезной инфекции (латентной или активной). Нет данных об увеличении риска реактивации туберкулезной инфекции при лечении моноклональными антителами к ИЛ-1 (например, препарата Иларис®). Перед применением препаратом Иларис® необходимо провести обследование всех пациентов с целью выявления активной или латентной туберкулезной инфекции (включая сбор анамнеза и проведение соответствующих скрининговых тестов, например туберкулиновой пробы, тестов IGRA (Interferon-Gamma-Release-Assay) или рентгенологического исследования грудной клетки. Во время лечения препаратом следует тщательно контролировать состояние пациентов с целью выявления туберкулезной инфекции. Рекомендовано информировать пациентов о необходимости обращаться к врачу при появлении следующих симптомов на фоне и после терапии препаратом Иларис® (длительно сохраняющийся кашель, потеря веса, субфебрильная температура). В случае конверсии туберкулинового теста из негативного в позитивный, особенно у пациентов высокого риска, необходимо провести альтернативные скрининговые тесты. При выявлении туберкулезной инфекции лечение препаратом Иларис® не следует начинать или продолжать.
Синдром активации макрофагов у пациентов с сЮИА
Синдром активации макрофагов - известное жизнеугрожающее состояние, которое может развиваться у пациентов с ревматическими заболеваниями, в частности у пациентов с сЮИА и требовать интенсивной терапии. Врачам следует внимательно относиться к симптомам инфекции или ухудшению течения сЮИА, известными как пусковой механизм для синдрома активации макрофагов. Данные клинических исследований указывают на то, что препарат Иларис® по всей вероятности не увеличивает риск развития синдрома активации макрофагов у пациентов с сЮИА, однако, не позволяет сделать окончательных выводов.
Препарат следует с осторожностью применять у пожилых пациентов; при наличии у больных в анамнезе рецидивирующих инфекций или любых состояний, предрасполагающих к развитию инфекции.
Передозировка
О подтвержденных случаях передозировки препаратом не сообщалось. При передозировке препаратом Иларис® следует обеспечить наблюдение за больным с целью выявления возможных нежелательных явлений, а также при необходимости назначить соответствующую симптоматическую терапию.Как хранить препарат
Хранить при температуре от 2 до 8 °С в защищенном от света месте.
Не замораживать.
Препарат следует хранить в недоступном для детей месте.
Срок годности
| Лиофилизат-3 года. Растворитель - 5 лет. Дата истечения срока годности комплекта определяется по более ранней д Условия отпускаПо рецептуИнформация по упаковкеI. Лиофилизат для приготовления раствора для подкожного введения Лиофилизат для приготовления раствора для подкожного введения 150 мг во флакон бесцветного стекла вместимостью 6 мл, укупоренный резиновой пробкой, обкатанный алюминиевым колпа Информация для врачей о препарате Иларис®Фармакологическая группаИммунодепрессивное средство, антитела моноклональные к интерлейкину-1?ФармакодинамикаКанакинумаб - полностью человеческое моноклональное антитело IgGl/каппа изотипа к интерлейкину-1?(ИЛ-1?). Канакинумаб с высоким аффинитетом связывается с человеческим ИЛ-1?, нейтрализуя, таким образом, его биологическое действие, блокируя взаимодействие ИЛ-1? с его рецепторами, ИЛ-1?-индуцированную активацию генов и продукцию медиаторов воспаления, таких как ИЛ-6 и циклооксигеназа-2. При лечении пациентов с системным ювенильным идиопатическим артритом (сЮИА) отмечалось быстрое и продолжительное улучшение суставных и системных проявлений заболевания: значительное уменьшение числа воспаленных суставов, быстрое исчезновение лихорадки и снижение реактантов острой фазы у большинства пациентов.У 33% пациентов на 29 день терапии отмечалось улучшение течения заболевания на 100% по педиатрическим критериям Американской коллегии ревматологов в сравнении с отсутствием эффекта в группе плацебо. Применение канакинумаба позволяет существенно снизить или отменить применение глюкокортикостероидов при терапии сЮИА. Канакинумаб позволяет удлинить временной промежуток до обострения заболевания, улучшить качество жизни пациентов и выполнение ими ежедневных задач. У пациентов с подагрическим артритом и различными фенотипами криопирин- ассоциированного периодического синдрома (cryopyrin-associated periodic syndrome, CAPS) включая семейный холодовой аутовоспалительный синдром/семейную холодовую крапивницу (Familial Cold Autoinflammatory Syndrome/ Familial Cold Urticaria, FCAS/FCU), Синдром Макл-Уэльса (Muckle-Wells Syndrome, MWS) и мультисистемное младенческое воспалительное заболевание/хронический младенческий неврологический кожно- артикулярный синдром (Neonatal onset multisystemic inflammatory disease/Chronic infantile neurological cutaneous and articular, NOMID/CINCA), канакинумаб снижает выраженность местных и системных воспалительных реакций, вызванных избыточной продукцией ИЛ-1?. При применении препарата у больных с острым приступом подагрического артрита снижается концентрация лабораторных маркеров воспаления (С реактивный белок (СРВ), сывороточного амилоида А (САА)), в течение короткого времени уходят признаки воспаления пораженного сустава (боль, отек, покраснение). На фоне применения препарата Иларис® 150 мг подкожно у пациентов с частыми обострениями приступов подагры (как минимум, 3 приступа в течение года) было отмечено статистически значимое снижение интенсивности боли (по шкале ВАШ) по сравнению с группой контроля (триамциналон 40 мг). На фоне применения препарата Иларис® снижение интенсивности боли наблюдается начиная с 24 часов после введения препаратов и в течение 7 дней после введения. При применении препарата Иларис® было продемонстрировано статистически значимое снижение риска возникновения нового приступа подагры на 62% в течение 12 недель терапии и на 56% в течение 24 недель терапии по сравнению с группой контроля. Эффективность препарата Иларис® при подагрическом артрите была сопоставима у пациентов в возрасте >65 и <65 лет. При применении канакинумаба у больных с различными фенотипами CAPS отмечается уменьшение уже в течение первых суток следующих проявлений заболевания: лихорадки, повышенной утомляемости, кожной сыпи, артралгии, миалгии, головной боли/мигрени, конъюнктивита, слабости, а также снижение (в течение нескольких дней) продукции маркеров воспаления, включая как СРВ и САА, и приводит к нормализации числа лейкоцитов и тромбоцитов (в случае их повышения). При длительном применении канакинумаба (в течение 48 недель) у пациентов с CAPS полный ответ на терапию, определяемый как сочетание уменьшения (до минимальной степени или полного исчезновения) симптомов аутовоспалительного заболевания и поражений кожи (сыпь по типу крапивницы), и снижения показателей СРВ и САА <10 мг/л, наблюдался в 97% случаев в течение 7-ми дней после начала терапии. При применении канакинумаба у больных не отмечалось развития рецидивов заболевания (в группе больных, получавших лечение плацебо, рецидивы наблюдались в 81% случаев). ФармакокинетикаАбсорбция У взрослых пациентов с различными фенотипами CAPS после однократного подкожного введения 150 мг препарата время достижения максимальной концентрации (Сmах) канакинумаба составляет около 7-ми дней. Средний конечный период полувыведения составляет 26 дней. При подкожном введении канакинумаба абсолютная биодоступность - 66% (популяционный фармакокинетический анализ у пациентов с CAPS, включая детей в возрасте от 2 лет). Параметры фармакокинетики (площадь под кривой "концентрация - время" (AUC) и максимальная концентрация (Сmах) повышаются пропорционально дозе в диапазоне доз от 0,30 до 10,0 мг/кг при внутривенной инфузии или при подкожном введении (в дозе от 150 до 600 мг). Распределение Канакинумаб связывается с сывороточным ИЛ-1?. Объем распределения (Vss) изменяется в зависимости от массы тела. У пациентов с CAPS Vss составляет 6,2 л при массе тела 70 кг, у пациентов с сЮИА - 3,2 л при массе тела 33 кг и у пациентов с подагрическим артритом - 7,9 л при массе тела 93 кг. При подкожном введении препарата в течение 6 месяцев в дозе 150 мг каждые 8 недель, в дозе 4 мг/кг каждые 4 недели, 150 мг каждые 12 недель коэффициент кумуляции канакинумаба составляет 1,3,1,6 и 1,1, соответственно. Выведение Клиренс (С1) изменяется в зависимости от массы тела. Для пациентов с CAPS этот показатель составляет 0,17 л/сут при массе тела 70 кг, у пациента с сЮИА 0,11 л/сут при массе тела 33 кг, у пациента с подагрическим артритом 0,23 л/сут при массе тела 93 кг. После учета весовых различий существенной разницы в фармакокинетических свойствах канакинумаба у пациентов с подагрическим артритом, различными фенотипами CAPS и сЮИА не было выявлено. При повторном применении препарата не наблюдается увеличения О или изменений каких-либо других, зависимых от времени фармакокинетических параметров канакинумаба. При назначении препарата с учетом массы тела пол и возраст пациентов не оказывают влияния на фармакокинетику препарата. Фармакокинетика в особых клинических случаях Пациенты в возрасте < 18 лет У пациентов в возрасте от 4 лет и старше после подкожного однократного введения препарата в дозе 150 мг или 2 мг/кг время достижения Сmах канакинумаба составляет 2-7 дней. Конечный период полувыведения канакинумаба у данной категории больных сходен с таковым у взрослых и составляет от 22,9 до 25,7 дней. Результаты популяционного анализа фармакокинетики канакинумаба у детей в возрасте от 2 до 4 лет сходны с таковыми у пациентов 4 лет и старше. Фармакокинетические характеристики у пациентов с CAPS и сЮИА схожи. При подкожном введении канакинумаба в дозе 4мг/кг каждые 4 недели у пациентов с сЮИА значения AUC и Сmах были аналогичны в возрастной группе от 2 до младше 20 лет. Пациенты в возрасте > 65 лет Не было выявлено разницы в фармакокинетических параметрах, основанных на С1 и Vss, у пациентов старшей возрастной группы и пациентов в возрасте менее 65 лет. Взаимодействие с другими веществамиСпециальных исследований по взаимодействию препарата Иларис® с другими лекарственными препаратами не проводилось. Поскольку экспрессия в печени изоферментов системы цитохрома Р450 может быть подавлена цитокинами, стимулирующими хроническое воспаление, такими как ИЛ-1?, то при назначении мощных ингибиторов цитокинов, экспрессия в печени изоферментов системы цитохрома Р450 может быть нормализована. Это является клинически значимым для препаратов, метаболизирующихся с помощью изоферментов системы цитохрома Р450 и имеющих узкий терапевтический индекс, когда доза препарата подбирается индивидуально. При назначении препарата Иларис® пациентам, принимающим такие препараты, их дозу следует при необходимости корректировать (в зависимости от их клинического эффекта и концентрации действующего вещества в плазме крови). В клинических исследованиях отмечено безопасное применение Иларис с противоподагрическими средствами. Препарат не рекомендуется назначать одновременно с ингибиторами ФНО и другими блокаторами ИЛ-1, поскольку их использование на фоне применения препарата Иларис® повышает риск развития тяжелых инфекций. Данные о влиянии вакцинации живыми вакцинами, а также о возможной вторичной передаче инфекции, пациентам, получающим лечение препаратом, отсутствуют. Вакцинировать больных, получающих лечение препаратом Иларис®, живыми вакцинами следует только в случае, когда польза от вакцинации превышает возможный риск. Рекомендуется, чтобы иммунизация была проведена (согласно календарю прививок) до начала терапии препаратом Иларис® (включая пневмококковую вакцину и инактивированную вакцину против гриппа). В случае необходимости вакцинацию живыми вакцинами проводят после начала терапии препаратом (по крайней мере, через 3 месяца после последней инъекции препарата и за 3 месяца до следующей). Данные проведенных клинических исследований на взрослых здоровых добровольцах показывают, что однократное введение Илариса в дозе 300 мг не влияет на начало выработки антител и персистенцию поствакцинального ответа при вакцинации против гриппа и менингококковой инфекции (гликозилированной белковой вакциной).
Смотрите также:
|