Герцептин® (Herceptin®)
1-Z А Б В Г Д Е - Ж - З И - Й К Л М Н О П Р С Т У Ф Х Ц Ч - Щ Э Ю - Я
Клинико-фармакологическая форма - трастузумаб
Форма выпуска
Раствор для подкожного введения 600 мг/5 мл.
Описание препарата Герцептин® (Herceptin®)
Прозрачная или опалесцирующая бесцветная или желтоватого цвета жидкость.Состав
1 флакон содержит:
действующее вещество: трастузумаб - 600 мг;
вспомогательные вещества: рекомбинантная человеческая гиалуронидаза (rHuPH20) - 10000 ЕД, L-гистидин - 1.95 мг, L-гистидина гидрохлорида моногидрат - 18.35 мг, ?,?- трегалозы дигидрат - 397.25 мг, L-метионин - 7.45 мг, полисорбат 20 - 2.0 мг, вода для инъекций до 5.0 мл.
Показания к применению
Метастатический рак молочной железы с опухолевой гиперэкспрессией HER2:
- в виде монотерапии, после одной или более схем химиотерапии;
- в комбинации с паклитакселом или доцетакселом, в случае отсутствия предшествующей химиотерапии (первая линия терапии);
- в комбинации с ингибиторами ароматазы при положительных гормональных рецепторах (эстрогеновых и/или прогестероновых) у женщин в постменопаузе.
Ранние стадии рака молочной железы с опухолевой гиперэкспрессией HER2:
- в виде адъювантной терапии после проведения хирургического вмешательства, завершения химиотерапии (неоадъювантной или адъювантной) и лучевой терапии;
- в комбинации с паклитакселом или доцетакселом после адъювантной химиотерапии доксорубицином и циклофосфамидом;
- в комбинации с адъювантной химиотерапией, состоящей из доцетаксела и карбоплатина;
- в комбинации с неоадъювантной химиотерапией и последующей адъювантной монотерапией препаратом Герцептин®, при местно-распространенном (включая воспалительную форму) заболевании или в случаях, когда размер опухоли превышает 2 см в диаметре.
Противопоказания к применению
Повышенная чувствительность к трастузумабу, белку мыши или любому компоненту препарата.
Беременность и период грудного вскармливания.
Детский возраст до 18 лет (эффективность и безопасность применения у детей не установлены).
Тяжелая одышка в покое, вызванная метастазами в легкие или требующая поддерживающей терапии кислородом.
Больные на ранних стадиях РМЖ с инфарктом миокарда в анамнезе, стенокардией, требующей лечения, хронической сердечной недостаточностью (II-IV функциональный класс по NYHA), ФВЛЖ <55%, кардиомиопатией, аритмией, клинически значимыми пороками сердца, неконтролируемой артериальной гипертензией, гемодинамически значимым перикардиальным выпотом (эффективность и безопасность применения препарата у данных групп пациентов не изучены); одновременное применение препарата с антрациклинами в составе адъювантной терапии у пациентов с ранними стадиями РМЖ.
Возможные побочные эффекты
ВНИМАНИЕ! Если вы подозреваете, что при приеме препарата ваше самочувствие ухудшилось, появились какие-то побочные эффекты, нужно сразу же обратиться очно к врачу, назначившему препарат!
В настоящее время наиболее серьезными и/или частыми нежелательными реакциями, о которых сообщалось при использовании препарата Герцептин®, являются: дисфункция сердца, реакции, связанные с введением, гематотоксичность (в частности, нейтропения), инфекции и нарушения со стороны легких.
Профиль безопасности препарата Герцептин® в лекарственной форме для подкожного введения при ранних стадиях РМЖ сопоставим с известным профилем безопасности для внутривенной лекарственной формы.
Некоторые нежелательные явления/реакции чаще развивались при использовании лекарственной формы для подкожного введения:
- Серьезные нежелательные явления (большинство из которых было связано с госпитализацией или продлением госпитализации): 14.1% при внутривенной форме введения в сравнении с 21.5% при подкожной форме введения. Различия по частоте серьезных нежелательных явлений между лекарственными формами наблюдались в основном за счет инфекций с/без нейтропении (4.4% против 8.1%) и кардиологических нарушений (0.7% против 1.7%).
- Инфекции послеоперационной раны (тяжелые и/или серьезные): 1.7% при внутривенной форме в сравнении с 3.0% при подкожной форме введения.
- Реакции, связанные с введением: 37.2% при внутривенной форме в сравнении с 47.8% при подкожной форме введения.
- Артериальная гипертензия: 4.7% для внутривенной формы в сравнении с 9.8 % для подкожной формы введения.
Для описания частоты нежелательных реакций в данном разделе используется следующая классификация: очень часто (>1/10), часто (>1/100, но <1/10), нечасто (>1/1000, но <1/100), редко (>1/10000, но <1/1000), очень редко (<1/10000), неизвестно (не может быть вычислена на основе имеющихся данных). В рамках каждой группы нежелательные реакции представлены в соответствии со снижением серьезности. Частота указана в соответствии с максимально встречавшейся в базовых клинических исследованиях.
Инфекционные и паразитарные заболевания: очень часто - назофарингит; часто - пневмония+, нейтропенический сепсис, цистит, Herpes zoster, инфекции, грипп, синусит, инфекции кожи, ринит, инфекции верхних дыхательных путей, инфекции мочевыводящих путей, рожа, воспаление подкожно-жировой клетчатки; нечасто - сепсис.
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы): неизвестно - прогрессирование злокачественного новообразования, прогресси- рование новообразования.
Нарушения со стороны крови и лимфатической системы: очень часто - фебрильная нейтропения, анемия, нейтропения, лейкопения, тромбоцитопения; неизвестно - гипопро- тромбинемия.
Нарушения со стороны иммунной системы: часто - реакции гиперчувствителыюсти; неизвестно - анафилактические реакции+, анафилактический шок+.
Нарушения со стороны обмена веществ: очень часто - снижение массы тела, анорексия; неизвестно - гиперкалиемия.
Нарушения психики: очень часто - бессонница; часто - тревога, депрессия, нарушение мышления.
Нарушения со стороны нервной системы: очень часто - тремор1, головокружение, головные боли, парестезии, дисгевзия (искажение вкусовых восприятий); часто - периферическая нейропатия, мышечный гипертонус, сонливость, атаксия; редко - парез; неизвестно - отек мозга.
Нарушения со стороны органа зрения: очень часто - конъюнктивит, повышенное слезоотделение; часто - сухость глаз; неизвестно - отек диска зрительного нерва, кровоизлияние в сетчатку.
Нарушения со стороны органа слуха и лабиринтные нарушения: нечасто - глухота.
Нарушения со стороны сердечно-сосудистой системы: очень часто - снижение и повышение артериального давления (АД)1, нарушение сердечного ритма1, сердцебиение1, трепетание (предсердий или желудочков)1, снижение фракции выброса левого желудочка*,
"приливы"; часто - сердечная недостаточность (хроническая)+, суправентрикулярная
тахиаритмия+1, кардиомиопатия, артериальная гипотензия+1, вазодилатация; нечасто
кардиальный выпот; неизвестно - кардиогенный шок, перикардит, брадикардия, ритм "галопа".
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения:
очень часто - хрипы+1, одышка+, кашель, носовое кровотечение, ринорея; часто - бронхиальная астма, нарушение функции легких, фарингит; нечасто - плевральный выпот+; редко - пневмонит; неизвестно - легочный фиброз+, дыхательная недостаточность+, инфильтрация легких+, острый отек легких+, острый респираторный дистресс-синдром+, бронхоспазм+, гипоксия+, снижение насыщения гемоглобина кислородом+, отек гортани, ортопноэ, отек легкого, интерстициальная болезнь легких.
Нарушения со стороны желудочно-кишечного тракта: очень часто - диарея, рвота, тошнота, отек губ1, боли в животе, диспепсия, запор, стоматит; часто - панкреатит, геморрой, сухость во рту.
Нарушения со стороны печени и желчевыводящих путей: часто - гепатит, болезненность в области печени, гепатоцеллюлярное повреждение; редко - желтуха; неизвестно - печеночная недостаточность.
Нарушения со стороны кожи и подкожных тканей: очень часто - эритема, сыпь, отек лица1, алопеция, нарушение структуры ногтей, ладонно-подошвенный синдром; часто - акне, сухость кожи, экхимоз, гипергидроз, макуло-папулезная сыпь, зуд, онихоклазия, дерматит; нечасто - крапивница; неизвестно - ангионевротический отек.
Нарушения со стороны костно-мышечной и соединительной ткани: очень часто - артралгия, мышечная скованность1, миалгия; часто - артрит, боли в спине, оссалгия, спазмы мышц, боль в области шеи, боли в конечностях.
Нарушения со стороны почек и мочевыводящих путей: часто - заболевание почек; неизвестно - мембранозный гломерулонефрит, гломерулонефропатия, почечная недостаточность.
Влияние на течение беременности, послеродовые и перинатальные состояния: неизвестно - олигогидрамнион, фатальная гипоплазия легких и гипоплазия и/или нарушение функции почек у плода.
Нарушения со стороны половых органов и молочной железы: часто - воспаление молочной железы/мастит.
Общие расстройства и нарушения в месте введения: очень часто - астения, боли в груди, озноб, слабость, гриппоподобный синдром, реакции, связанные с введением препарата, боли, лихорадка, мукозит, периферические отеки; часто - недомогание, отеки.
Травмы, интоксикации и осложнения манипуляций: часто - ушиб.
+ - нежелательные реакции, которые в сообщениях ассоциировались с летальным исходом.
1 - нежелательные реакции, которые в основном сообщались в ассоциации с реакциями на введение. Точное процентное количество не установлено.
* - нежелательные реакции наблюдались при комбинированной терапии после антрацик- линов и в комбинации с таксанами.
Ниже представлена информация по отдельным нежелательным реакциям.
Дисфункция сердца
Хроническая сердечная недостаточность (ХСН) II-IV функционального класса по NYHA (классификация Нью-Йоркской Ассоциации Кардиологов) является частой нежелательной реакцией при применении препарата Герцептин® и ассоциировалась с фатальным исходом. У пациентов, получавших препарат Герцептин®, наблюдались следующие признаки и симптомы нарушения функции сердца: одышка, ортопноэ, усиление кашля, отек легких, ритм "галопа" или снижение фракции выброса левого желудочка. В 3 базовых клинических исследованиях применения трастузумаба в/в в комбинации с адъювантной химиотерапией частота сердечной дисфункции 3/4 степени (а именно симптоматическая хроническая сердечная недостаточность) не отличалась от таковой у пациентов, получавших только химиотерапию (т.е. без препарата Герцептин®), и у пациентов, получавших таксаны и Герцептин® последовательно (0.3-0.4%). Частота была наибольшей у пациентов, получавших Герцептин® совместно с таксанами (2.0%). Опыт использования препарата Герцептин® в комбинации с низкодозовыми режимами антрациклинов в неоадъювантной терапии ограничен.
При применении препарата Герцептин® в течение одного года после завершения адъювантной химиотерапии, сердечная недостаточность III-IV функционального класса по NYHA наблюдалась у 0.6% пациентов при медиане наблюдения 12 месяцев и у 0.89% пациентов при медиане наблюдения 8 лет. Частота легкой симптоматической и бессимптомной дисфункции левого желудочка составила 6.35%. Тяжелая ХСН была обратима в 70% случаев (обратимость определялась как минимум два последовательных повышения показателя ФВЛЖ >50% после явления). Легкая симптоматическая и бессимптомная дисфункция левого желудочка была обратима в 83.1% случаев. Приблизительно 10% явлений, связанных с дисфункцией сердца, возникли после завершения терапии препаратом Герцептин®.
В базовых клинических исследованиях при метастатическом РМЖ частота сердечной дисфункции при внутривенном введении препарата Герцептин® в сочетании с паклитакселом варьировала от 9% до 12% по сравнению с 1%-4% для монотерпии пакли гакселом. Для монотерапии препаратом Герцептин® частота составила 6%-9%. Наибольшая частота сердечной дисфункции наблюдалась у пациентов, получающих Герцептин® одновременно с антрациклинами/циклофосфамидом (27%), что значительно выше, чем для терапии антрациклинами /циклофосфамидом (7%-10%).
В исследовании с проспективным мониторингом функции сердца, частота симптоматической ХСН составила 2.2% у пациентов, получавших препараты Герцептин® и доцетаксел по сравнению с 0% у пациентов, получавших монотерапию доцетакселом. У большинства пациентов (79%) с сердечной дисфункцией наблюдалось улучшение состояния после получения стандартной терапии ХСН.
Реакции, связанные с введением, и реакции гиперчувствительности
Реакции, связанные с введением/реакции гиперчувствительности, такие как озноб и/или лихорадка, одышка, артериальная гипотензия, хрипы в легких, бронхоспазм, тахикардия, снижение насыщения гемоглобина кислородом, респираторный дистресс-синдром, сыпь, тошнота, рвота и головная боль наблюдались при применении препарата Герцептин®.
Частота реакций на введение всех степеней тяжести варьирует и зависит от показания,
методологии сбора информации, а также от того вводился ли Герцептин® совместно с химиотерапией или применялся в монотерапии.
При сравнении препарата Герцептин® в лекарственной форме для внутривенного введения с лекарственной формой для подкожного введения частота реакций, связанных с введением, всех степеней тяжести составила 37.2% и 47.8%, соответственно. Среди тяжелых реакций наблюдались только явления 3 степени тяжести у 2.0% и 1.7% пациентов, соответственно. Реакции 4 и 5 степени тяжести не зарегистрированы. Все тяжелые реакции при
применении препарата Герцептин® подкожно развивались на фоне совместного применения химиотерапии. Наиболее частой тяжелой реакцией была лекарственная гиперчувствительность. Системные реакции включали гиперчувствительность, артериальную гипотензию, тахикардию, кашель и одышку. Местные реакции включали покраснение, зуд, отек и сыпь в месте введения.
Гематологическая токсичность
Очень часто возникала фебрильная нейтропения. Нежелательные реакции, возникающие часто, включают в себя анемию, лейкопению, тромбоцитопению и нейтропению. Частота возникновения гипопротромбинемии неизвестна. Риск нейтропении может быть несколько выше при применении трастузумаба в комбинации с доцетакселом после терапии препаратами антрациклинового ряда.
Нарушения со стороны легких
С применением препарата Герцептин® ассоциируются тяжелые нежелательные явления со стороны легких (в том числе с фатальным исходом). Данные реакции включают в себя (но не ограничиваются): инфильтраты в легких, острый респираторный дистресс-синдром, пневмонию, пневмонит, плевральный выпот, острый отек легких и дыхательную недостаточность.
Инфекции
Частота тяжелых инфекций (>3 степени тяжести в соответствии с общими критериями
токсичности Национального института рака в США (NCI СТСАЕ) версия 3.0) составляет 5.0% для препарата Герцептин® в лекарственной форме для внутривенного введения по сравнению с 7.1% для препарата Герцептин® в лекарственной форме для подкожного введения.
Частота серьезных инфекций (большинство из которых было связано с госпитализацией или продлением госпитализации) составляет 4.4% при внутривенном применении препарата Герцептин® и 8.1% при подкожном. Разница между лекарственными формами наблюдалась в основном в рамках фазы адъювантной терапии (монотерапии) и в основном за счет инфекций послеоперационных ран, хотя имелись различия и по частоте других инфекций, таких как инфекции дыхательных путей, острый пиелонефрит и сепсис. Все явления разрешились в среднем в течение 13 дней при применении препарата Герцептин® в лекарственной форме для внутривенного введения и в течение 17 дней при применении препарата Герцептин® в лекарственной форме для подкожного введения.
Повышение артериального давления
Частота повышения артериального давления на фоне применения препарата Герцептин® в лекарственной форме для подкожного введения в два раза выше по сравнению с применением в лекарственной форме для внутривенного введения (4.7% по сравнению с 9.8%). При этом доля пациентов с тяжелыми явлениями (NCI СТСАЕ >3 степени) больше среди пациентов, получавших препарат Герцептин® в лекарственной форме для подкожного введения (2.0%) по сравнению с <1% в группе пациентов, получавших препарат в лекарственной форме для внутривенного введения. Все пациенты, сообщившие о тяжелой артериальной гипертензии, кроме одного, имели артериальную гипертензию в анамнезе до включения в исследование. Развитие тяжелых нежелательных явлений повышения артериального давления возможно как в день инъекции, так и в последующие дни.
Дозировка, как принимать Герцептин® (Herceptin®)
Тестирование на опухолевую экспрессию HER2 до начала лечения препаратом Герцептин® является обязательным.
Лечение препаратом Герцептин® должно проводиться только под наблюдением врача, имеющего опыт применения цитотоксической химиотерапии.
Препарат должен вводиться медицинским персоналом, соблюдая асептические условия. Перед введением препарата важно проверить его маркировку и убедиться, что лекарственная форма препарата соответствует назначению - для подкожного введения.
Герцептин® в лекарственной форме "раствор для подкожного введения" не предназначен для внутривенного введения и должен применяться только подкожно!
В настоящее время информация о переходе с одной лекарственной формы на другую ограничена.
Препарат Герцептин® в лекарственной форме "для подкожного введения" является готовым к использованию раствором, который нельзя растворять в других лекарственных препаратах или смешивать.
Перед введением раствор следует проверить (визуально) на предмет отсутствия механических примесей и изменения окраски.
Правила хранения раствора для подкожного введения после забора в шприц Так как раствор препарата Герцептин® для подкожного введения не содержит антимикробного консерванта, с микробиологической точки зрения препарат должен быть использован сразу после вскрытия флакона и забора в шприц.
После забора в шприц лекарственный препарат сохраняет физическую и химическую стабильность в течение 48 часов при температуре 2-8°С и в течение 6 часов при комнатной температуре (максимально 30°С) при рассеянном дневном освещении, при условии, что набор препарата в шприц проводится в контролируемых, валидированных асептических условиях. Если препарат во флаконе уже хранился какое-то время при комнатной температуре, то хранить препарат, набранный в шприц, при комнатной температуре нельзя. После набора раствора в шприц рекомендуется заменить иглу-переходник на закрывающий колпачок шприца во избежание высыхания раствора в игле и снижения качества лекарственного препарата. Игла для подкожного введения должна быть присоединена к шприцу непосредственно перед введением с корректировкой объема раствора до 5 мл. Флакон с препаратом используется только однократно.Стандартный режим дозирования
Подкожно (п/к), в фиксированной дозе 600 мг/5 мл (независимо от массы тела пациента), в течение 2-5 минут, каждые 3 недели. Нагрузочная доза не требуется.
Инъекции следует производить попеременно в левое и правое бедро. Место новой инъекции должно отстоять от предыдущего минимум на 2.5 см и не затрагивать участки покраснения, синяков, болезненности и уплотнений. Для подкожного введения других препаратов следует использовать другие места введения.
Продолжительность терапии
Лечение препаратом Герцептин® у пациентов с метастатическим РМЖ проводится до про- грессирования заболевания. Пациенты с ранними стадиями РМЖ должны получать терапию препаратом Герцептин® в течение 1 года или до рецидива заболевания (в зависимости от того, что произойдет быстрее). Лечение препаратом Герцептин® пациентов с ранними стадиями РМЖ свыше одного года не рекомендуется.
Коррекция дозы
В период возникновения обратимой миелосупрессии, вызванной химиотерапией, курс терапии препаратом Герцептин® может быть продолжен после снижения дозы химиотерапии или временной ее отмены (согласно соответствующим рекомендациям в инструкциях по применению паклитаксела, доцетаксела или ингибитора ароматазы), при условии тщательного контроля осложнений, обусловленных нейтропенией.
При снижении фракции выброса левого желудочка (ФВЛЖ) на >10 единиц от исходной И ниже значения 50% лечение должно быть приостановлено. Повторная оценка ФВЛЖ должна быть проведена приблизительно через 3 недели. При отсутствии улучшения показателя ФВЛЖ, или его дальнейшем снижении, или появления симптомов хронической сердечной недостаточности (ХСН) необходимо рассмотреть вопрос о прекращении лечения препаратом Герцептин®, если только польза для конкретного пациента не превосходит риски. Все эти пациенты должны быть направлены к кардиологу для проведения обследования и находиться под наблюдением. Пропуск в плановом введении
При пропуске фиксированной дозы препарата Герцептин® для подкожного введения следует как можно быстрее ввести следующую (т.е. пропущенную) дозу 600 мг. Интервал между следующими подряд инъекциями препарата Герцептин® для подкожного введения не должен быть менее 3 недель.
Особые указания по дозированию
Пациенты пожилого возраста
Снижение дозы препарата Герцептин® у больных пожилого возраста не требуется.
Влияние на беременность
Применение препарата во время беременности и в период грудного вскармливания противопоказано.
Женщинам детородного возраста во время лечения препаратом Герцептин® и, как минимум, в течение 7 месяцев после окончания лечения необходимо использовать надежные методы контрацепции.
В случае наступления беременности необходимо предупредить женщину о возможности вредного воздействия на плод. Если беременная продолжит получать терапию препаратом Герцептин®, то она должна находиться под тщательным наблюдением врачей разных специальностей. Неизвестно, влияет ли Герцептин® на репродуктивную способность у женщин. Результаты экспериментов на животных при применении препарата Герцептин® внутривенно не выявили признаков нарушения фертильности или негативного влияния на плод.
Вскармливание грудным молоком не рекомендуется во время лечения и, как минимум, в течение 7 месяцев после окончания терапии препаратом Герцептин®.
Управление транспортом
Исследования по изучению влияния препарата на способность управлять автомобилем и работать с механизмами не проводились. В случае возникновения реакций, связанных с введением препарата, пациентам не следует управлять автомобилем или работать с механизмами до полного разрешения симптомов.Дополнительные указания при приеме Герцептин®
В медицинской документации больного следует указывать торговое наименование препарата. Замена препарата на какой-либо другой биологический лекарственный препарат требует согласования с лечащим врачом.
HER2 тестирование должно быть проведено в специализированной лаборатории, которая
может обеспечить контроль качества процедуры тестирования.
Герцептин® должен использоваться у пациентов с метастатическим РМЖ или ранними стадиями РМЖ только при наличии опухолевой гиперэкспрессии HER2, определенной методом иммуно-гистохимической реакции (ИГХ), или амплификации гена HER.2, определенной методом гибридизации in situ (FISH или CISH). Следует использовать точные и валидированные методы определения.
В настоящее время отсутствуют данные из клинических исследований о пациентах, получавших Герцептин® повторно после применения в адъювантной терапии.
Дисфункция сердца
Пациенты, получающие Герцептин® в качестве монотерапии или в комбинации с
паклитакселом или доцетакселом, особенно после химиотерапии, включающей антрациклины (доксорубицин или эпирубицин), имеют повышенный риск развития хронической сердечной недостаточности (ХСН) (II-IV функциональный класс по NYHA) или бессимптомных нарушений функции сердца. Тяжесть этих явлений может варьировать от средней до тяжелой степени. Эти явления могут привести к смертельному исходу. Кроме этого, необходимо соблюдать осторожность при лечении пациентов с высоким сердечно-сосудистым риском, например, у пациентов пожилого возраста, с артериальной гипертензией, документально подтвержденной ишемической болезнью сердца, хронической сердечной недостаточностью, фракцией выброса левого желудочка (ФВЛЖ) <55%.
Больные, которым планируется назначение препарата Герцептин®, особенно те из них, которые ранее получали препараты антрациклинового ряда и циклофосфамид, должны вначале пройти тщательное кардиологическое обследование, включающее сбор анамнеза, физикальный осмотр, электрокардиографию, эхокардиографию (ЭКГ) и/или радиоизотопную вентрикулографию (MUGA) или магнитно-резонансную томографию (МРТ).
Мониторирование может позволить выявить пациентов с возникшими нарушениями функции сердца. Исходно проведенное кардиологическое обследование должно повторяться каждые 3 месяца во время терапии и каждые 6 месяцев после ее окончания в течение 24 месяцев с момента введения последней дозы препарата.
До начала лечения препаратом Герцептин® необходимо тщательно сопоставить возможную пользу и риск от его применения.
Поскольку период полувыведения трастузумаба составляет около 28-38 дней, препарат может находиться в крови до 27 недель после завершения терапии. У пациентов, которые получают антрациклины после завершения лечения препаратом Герцептин®, возможно повышение риска дисфункции сердца. По возможности врачи должны избегать назначения химиотерапии на основе антрациклинов в течение 27 недель после завершения терапии препаратом Герцептин®.
При применении препаратов антрациклинового ряда следует проводить тщательный мониторинг функции сердца.
Следует оценить необходимость проведения стандартного кардиологического обследования у пациентов с подозрением на сердечно-сосудистые заболевания. У всех пациентов следует мониторировать функцию сердца во время лечения (например, каждые 12 недель).
В результате мониторинга можно выявить пациентов, у которых развились нарушения функции сердца.
У пациентов с бессимптомным нарушением функции сердца может оказаться полезным более частое проведение мониторинга (например, каждые 6-8 недель). При продолжительном ухудшении функции левого желудочка, не проявляющемся симптоматически, целесообразно рассмотреть вопрос об отмене препарата, если клиническая польза от его применения отсутствует. Безопасность продолжения или возобновления терапии препаратом Герцептин® у пациентов, у которых развилось нарушение функции сердца, не изучалась.
При снижении фракции выброса левого желудочка (ФВЛЖ) на >10 единиц от исходной И ниже значения 50% лечение должно быть приостановлено. Повторная оценка ФВЛЖ должна быть проведена приблизительно через 3 недели. При отсутствии улучшения показателя ФВЛЖ, или его дальнейшем снижении, или при появлении симптомов хронической сердечной недостаточности (ХСН) необходимо рассмотреть вопрос о прекращении лечения препаратом Герцептин®, если только польза для конкретного пациента не превосходит риски. Все эти пациенты должны быть направлены к кардиологу для проведения обследования и находиться под наблюдением.
Если на фоне терапии препаратом Герцептин® развивается симптоматическая сердечная недостаточность, необходимо провести соответствующую стандартную медикаментозную терапию ХСН. У большинства пациентов с ХСН или бессимптомной дисфункцией сердца в базовых исследованиях наблюдалось улучшение состояния на фоне стандартной медикаментозной терапии ХСН: ингибиторы ангиотензинпревращающего фермента или
блокаторы рецепторов ангиотензина и бета-адреноблокаторы. При наличии клинической пользы от применения препарата Герцептин® большинство пациентов с побочными реакциями со стороны сердца продолжили терапию без проявления дополнительных клинически значимых реакций со стороны сердца.
Метастатический рак молочной железы
Не рекомендуется применять препарат Герцептин® совместно в комбинации с антрацик- линами для лечения метастатического рака молочной железы.
Риск развития дисфункции сердца у пациентов с метастатическим раком молочной железы повышен при предшествующей терапии антрациклинами, однако он ниже по сравнению с таковым при одновременном применении антрациклинов и препарата Герцептин®.
Ранние стадии рака молочной железы
Пациентам с ранними стадиями рака молочной железы следует проводить кардиологическое обследование перед началом лечения, каждые 3 месяца во время терапии и каждые 6 месяцев после ее окончания в течение 24 месяцев с момента введения последней дозы препарата. Рекомендуется более длительный мониторинг после лечения препаратом Герцептин® в комбинации с антрациклинами с частотой обследований 1 раз в год в течение 5 лет с момента введения последней дозы препарата Герцептин® или далее, если наблюдается постоянное снижение ФВЛЖ.
Лечение препаратом Герцептин® не рекомендуется больным на ранних стадиях РМЖ (адъювантная и неоадъювантная терапия) с: инфарктом миокарда в анамнезе; стенокардией, требующей лечения; ХСН (II-IV функциональный класс по NYHA) в анамнезе или в настоящее время; ФВЛЖ ниже 55%; другими кардиомиопатиями; аритмиями, требующими лечения; клинически значимыми пороками сердца; плохо контролируемой артериальной гипертензией, за исключением артериальной гипертензии, поддающейся стандартной медикаментозной терапии; и гемодинамически значимым перикардиальным выпотом, поскольку эффективность и безопасность применения препарата у таких пациентов не изучены.
Адъювантная терапия
Не рекомендуется применять препарат Герцептин® совместно в комбинации с антрациклинами в составе адъювантной терапии. У пациентов с ранними стадиями РМЖ, получавших Герцептин® (в/в) после химиотерапии на основе антрациклинов, наблюдалось повышение частоты симптоматических и бессимптомных нежелательных явлений со стороны сердца по сравнению с таковыми, получавшими химиотерапию доцетакселом и карбо- платином (режимы, не содержащие препараты антрациклинового ряда). При этом разница была больше в случаях совместного применения препарата Герцептин® и таксанов, чем при последовательном использовании.
Независимо от использовавшегося режима, большинство симптоматических кардиальных явлений возникало в первые 18 месяцев лечения. Продолжительное увеличение кумулятивной частоты симптоматических кардиальных явлений или явлений, связанных со снижением фракции выброса левого желудочка (ФВЛЖ) наблюдаетсяу 2.37% пациентов, получавших Герцептин® совместно с таксанами после терапии антрациклинами, но сравнению с 1% пациентов в группах сравнения (в группе терапии антрациклинами и циклофосфамидом, далее таксанами, и в группе терапии таксанами, карбоплатином и препаратом Герцептин®).
Идентифицированными факторами риска развития нежелательных явлений со стороны сердца при адъювантной терапии препаратом Герцептин® являются: возраст >50 лет, низкая исходная ФВЛЖ (<55%) перед и после начала лечения паклитакселом, снижение ФВЛЖ на 10-15 единиц, предшествующий или сопутствующий прием антигипертензивных препаратов.
Риск нарушения сердечной функции у пациентов, получавщих Герцептин® после завершения адъювантной химиотерапии, ассоциировался с более высокой суммарной дозой антрациклинов перед началом лечения препаратом Герцептин® и с индексом массы тела (ИМТ) >25 кг/м2.
Неоадъювантная-адъювантная терапия
Для пациентов с ранними стадиями РМЖ, которым может быть назначена неоадъювантная-адъювантная терапия, применение препарата Герцептин® совместно с антрациклинами рекомендовано только в случае, если они ранее не получали химиотерапию и только при использовании низкодозовых режимов терапии антрациклинами (максимальная суммарная доза доксорубицина 180 мг/м2 или эпирубицина 360 мг/м2).
У пациентов, получивших полный курс низкодозовых антрациклинов и Герцептин® в составе неоадъювантной терапии, не рекомендуется проведение дополнительной цитотоксической химиотерапии после проведения хирургического вмешательства. Во всех других случаях решение о необходимости дополнительной цитотоксической химиотерапии принимается на основании индивидуальных факторов.
Опыт применения трастузумаба совместно с низкодозовыми режимами терапии
антрациклинами ограничен двумя исследованиями. При применении препарата Герцептин® совместно с неоадъювантной химиотерапией, включавшей от трех до четырех циклов неоадъювантной терапии антрациклинами (суммарная доза доксорубицина 180 мг/м2 или
эпирубицина 300 мг/м2), частота симптоматического нарушения функции сердца была низкой (1.7%).
Клинический опыт применения у пациентов в возрасте старше 65 лет ограничен.
Реакции, связанные с введением
Для снижения риска возникновения реакций на введение может использоваться премедикация.
Несмотря на то, что серьезных реакций (включающих одышку, артериальную гипотензию, хрипы в легких, бронхоспазм, тахикардию, снижение насыщения гемоглобина кислородом и респираторный дистресс-синдром), связанных с введением, для препарата Герцептин® в лекарственной форме для подкожного введения не зарегистрировано, необходимо соблюдать осторожность, поскольку данные явления наблюдались при введении внутривенной лекарственной формы препарата Герцептин®.
Возможен прием анальгетиков/антипиретиков, таких как парацетамол, или антигистамин- ных препаратов, таких как дифенгидрамин. Серьезные реакции, связанные с а внутривенным введением препарата Герцептин®, успешно поддавались лечению, заключавшемуся в применении бета-адреностимуляторов, глюкокортикостероидов, ингаляции кислорода. В редких случаях данные реакции ассоциировались с фатальным исходом. Риск развития летальных реакций, связанных с введением, выше у пациентов с одышкой в покое, вызванной метастазами в легкие или сопутствующими заболеваниями, поэтому таким больным не следует проводить терапию препаратом Герцептин®.
Нарушения со стороны легких
Следует соблюдать осторожность при применении препарата Герцептин® в лекарственной форме для подкожного введения, т.к. при использовании препарата Герцептин® в лекарственной форме для внутривенного введения в пострегистрационном периоде регистрировались тяжелые явления со стороны легких, которые иногда сопровождались летальным исходом. Данные явления могут возникнуть как при введении препарата, так и отсрочено. Кроме того, наблюдались случаи интерстициальной болезни легких (ИБЛ). включая легочные инфильтраты, острый респираторный дистресс-синдром, пневмонию, пневмонит, плевральный выпот, острый отек легких и дыхательную недостаточность. Факторы риска, ассоциированные с ИБЛ, включают ранее проводимую или сопутствующую терапию другими противоопухолевыми препаратами, которые, как известно, связаны с ИБЛ (таксаны, гемцитабин, винорельбин и лучевая терапия). Риск тяжелых реакций со стороны легких выше у пациентов с метастатическим поражением легких, сопутствующими заболеваниями, сопровождающимися одышкой в покое, поэтому такие пациенты не должны получать препарат Герцептин®. Следует соблюдать осторожность, особенно у пациентов, получающих сопутствующую терапию таксанами, из-за возможности развития пневмонита.
Иглы и шприцы нельзя использовать повторно. Использованные иглы и шприцы помещают в защищенный от проколов контейнер (емкость). Утилизацию препарата Герцептин® и расходных материалов следует проводить в соответствии с местными требованиями.
Ишемическая болезнь сердца, артериальная гипертензия, сердечная недостаточность, сопутствующие заболевания легких или метастазы в легкие, предшествующая терапия кардиотоксичными лекарственными средствами, в т.ч. антрациклинами/циклофосфамидом, фракция выброса левого желудочка (ФВЛЖ) <50%, пожилой возраст.Передозировка
Введение препарата Герцептин® в лекарственной форме для подкожного введения в разовых дозах до 960 мг не сопровождалось нежелательными явлениями.
Как хранить препарат
При температуре 2-8°С в защищенном от света месте. Хранить в недоступном для детей месте. Не замораживать.Срок годности
1 год 9 месяцев. Не использовать по истечении срока годности, указанного на упаковке.
Условия отпуска
По рецептуИнформация по упаковке
По 600 мг/5 мл препарата во флакон бесцветного стекла (гидролитический класс 1 ЕФ), укупоренный пробкой из бутилкаучука, ламинированного фторполимером, обжатый алюминиевым колпачком и закрытый пластмассовой крышкой.
1 флакон с препаратом вме
Информация для врачей о препарате Герцептин®
Фармакологическая группа
Противоопухолевое средство - моноклональные антитела.Фармакодинамика
Трастузумаб представляет собой рекомбинантные ДНК-производные гуманизированные моноклональные антитела, которые избирательно взаимодействуют с внеклеточным доменом рецепторов эпидермального фактора роста человека 2 типа (HER2). Эти антитела представляют собой IgG1, состоящие из человеческих регионов (константные участки тяжелых цепей) и определяющих комплементарность мышиных участков антитела p185 HER2 к HER2.
Прото-онкоген HER2 или с-егВ2 кодирует трансмембранный рецептороподобный белок с молекулярной массой 185 кДа, который структурно подобен другим членам семейства рецепторов эпидермального ростового фактора. Гиперэкспрессия HER2 обнаруживается в ткани первичного рака молочной железы (РМЖ) у 15-20% больных. Амплификация гена HER2 приводит к гиперэкспрессии белка HER2 на мембране клеток опухоли, что в свою очередь вызывает постоянную активацию рецептора HER2. Внеклеточный домен рецептора (ECD, p105) может попадать ("слущиваться") в кровоток и определяться в образцах сыворотки крови.
Исследования показывают, что больные раком молочной железы, у которых отмечена амплификация или гиперэкспрессия HER2 в ткани опухоли, обладают меньшей выживаемостью без признаков заболевания по сравнению с больными без амплификации или гиперэкспрессии HER2 в ткани опухоли.
Трастузумаб блокирует пролиферацию опухолевых клеток человека с гиперэкспрессией HER2 in vivo и in vitro. In vitro антитело-зависимая клеточная цитотоксичность трастузумаба преимущественно направлена на опухолевые клетки с гиперэкспрессией HER2.
Иммуногенность
При неоадъювантной и адъювантной терапии препаратом Герцептин® у 14.6% пациентов, получавших препарат в лекарственной форме для подкожного введения, образовывались антитела к трастузумабу (включая пациентов, у которых антитела к трастузумабу обнаруживались до лечения).
Клиническая значимость наличия антител к трастузумабу неизвестна. Не отмечено нежелательного влияния данных антител на фармакокинетику, эффективность (определяемую по полному патологическому ответу) или безопасность (определяемую по частоте реакций, связанных с введением) препарата Герцептин®.
Фармакокинетика
Фармакокинетика трастузумаба, вводимого подкожно в дозе 600 мг каждые 3 недели, сравнивалась с таковой при внутривенном введении (8 мг/кг нагрузочная доза, затем введение поддерживающей дозы 6 мг/кг каждые 3 недели). Установлено, что при подкожном применении фиксированной дозы препарата Герцептин® минимальная концентраци (Ctrough) перед 8 циклом соответствует таковой при применении препарата Герцептин® для внутривенного введения в дозе, скорректированной по массе тела.В течение периода неоадъювантной терапии среднее значение Ctrough перед введением следующей дозы 8 цикла было выше при подкожном введении трастузумаба (78.7 мкг/мл) по сравнению с таковой при внутривенном введении (57.8 мкг/мл). Во время адъювантной терапии средние значения Ctrough перед введением следующей дозы 13 курса составили 90.4 мкг/мл при подкожном введении и 62.1 мкг/мл при внутривенном введении трастузумаба. В то время как равновесная концентрация при внутривенном введении достигается после 8 курса, при подкожном введении концентрации имеют тенденцию к нарастанию до 13 курса. Медиана времени достижения максимальной концентрации (Тmах) после подкожного введения составила приблизительно 3 дня с высокой индивидуальной вариабельностью (в диапазоне 1-14 дней). Среднее значение максимальной концентрации (Сmах) было, как и ожидалось, более низким при введении трастузумаба подкожно (149 мкг/мл), чем при внутривенном введении (значение на момент окончания инфузии 221 мкг/мл). Среднее значение площади под кривой "концентрация-время" (AUC0-21 дней) после 7 курса было приблизительно на 10% выше при подкожном введении трастузумаба по сравнению с внутривенной формой (AUC 2268 мкг/мл х день и 2056 мкг/мл х день, соответственно). В связи с выраженным влиянием массы тела на клиренс трастузумаба и с использованием фиксированной дозы для подкожного введения, разница в экспозициях между подкожной и внутривенной лекарственной формой зависит от массы тела: у пациентов с массой тела <51 кг среднее равновесное значение AUC трастузумаба примерно на 80% выше при внутривенном введении, чем при подкожном введении, тогда как при массе тела >90 кг значение AUC на 20% ниже после подкожного введения по сравнению с внутривенным. По данным популяционного фармакокинетического анализа (модель с параллельным линейным и нелинейным выведением из центральной камеры) расчетная биодоступность при подкожном введении составила 77.1%, линейный клиренс (СL) - 0.111 л/день и объем распределения в центральной камере (Vc) - 2.91 л. Значения нелинейных параметров выведения по модели Михаэлиса-Ментена составили 11.9 мг/день для максимальной скорости (Vmax) и 33.9 мг/л для константы (Km). Результаты популяционного фармакокинетического моделирования показали, что изменение дозы в зависимости от массы тела не требуется.
Фармакокинетика у особых групп пациентов
Отдельные фармакокннетические исследования у пациентов пожилого возраста и пациентов с почечной или печеночной недостаточностью не проводились.
Пожилой возраст
Возраст не влияет на распределение трастузумаба.
Взаимодействие с другими веществами
Специальные исследования лекарственных взаимодействий препарата Герцептин® не проводились.
В клинических исследованиях клинически значимых взаимодействий с одновременно применяемыми препаратами не отмечалось.
При применении трастузумаба в комбинации с доцетакселом, карбоплатином или анастрозолом, фармакокинетические параметры данных препаратов, включая трастузумаб, не изменялись.
Концентрация паклитаксела и доксорубицина (и их основных метаболитов 6-альфа-гидроксипаклитаксел и доксорубицинол) в присутствии трастузумаба не изменялась. Тем не менее, трастузумаб может повысить общую экспозицию одного из метаболитов доксорубицина (7-дезокси-13-дигидродоксорубицинон). Биологическая активность этого метаболита и клиническое значение повышения его экспозиции неизвестны. Результаты изучения фармакокинетики капецитабина и цисплатина при использовании в комбинации с трастузумабом или без него предполагают, что экспозиция биологически активных метаболитов капецитабина (например, фторурацил) не изменялась при одновременном применении цисплатина или цисплатина и трастузумаба. Однако были зарегистрированы более высокие концентрации капецитабина и более длительный период его полувыведения при комбинации с трастузумабом. Данные также указывают, что фармакокинетика цисплатина не изменялась при одновременном применении капецитабина или капецитабина в комбинации с трастузумабом.
Препарат Герцептин® в лекарственной форме для подкожного введения является готовым к использованию раствором, который нельзя растворять в других лекарственных препаратах или смешивать.
Признаков несовместимости между раствором препарата Герцептин® для подкожного введения и шприцами из полипропилена не наблюдалось.

Секреты долголетия: уроки из синих зон Земли

Влияние микропластика на здоровье: что говорят эксперты

Новый подход к менопаузе: заморозка ткани яичника может изменить все

Омега-3 vs. витамин D: что выбрать для здоровья иммунной системы?

Сможем ли мы добавить больше активной жизни к нашим годам?

Новое исследование: как фантазии помогают укрепить память
 Боли в грудной клетке при заболеваниях желудка
Боли в грудной клетке при заболеваниях желудка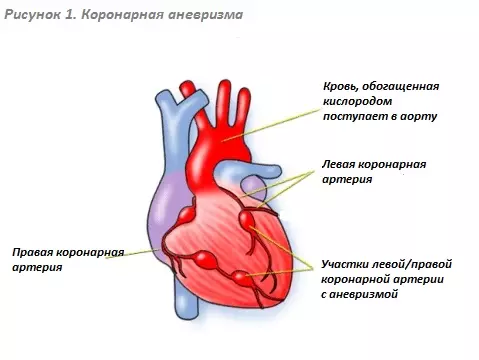 Аневризма коронарной артерии
Аневризма коронарной артерии Лечение хронической сердечной недостаточности
Лечение хронической сердечной недостаточности Первая помощь при сердечном приступе, прием нитроглицерина
Первая помощь при сердечном приступе, прием нитроглицерина

